Kontakty
Rychlý kontakt (24h)
+420 543 131 111
Nový onkologický pacient
+420 543 135 809
Zdravotnická pracoviště
Pro zdravotníky a odborníky
Stáže a výuka
Mezioborové indikační komise
Úsek podpory zdravotnických týmů a komisí
Odbor nelékařských zdravotnických pracovníků
Odbor léčebně-preventivní péče
Nezdravotnická pracoviště
Vedení nemocnice
Ekonomický odbor
Oddělení personální a mzdové
Právní oddělení
Oddělení informatiky
Odbor kanceláře ředitele
Odbor hospodářsko-technických služeb
Úsek zdravotních pojišťoven
Úsek tiskového mluvčího
Etická komise
Odbor vědy, výzkumu a vzdělávání
Centrální kartotéka a příjem
Úsek radiační ochrany
Úsek interního auditu
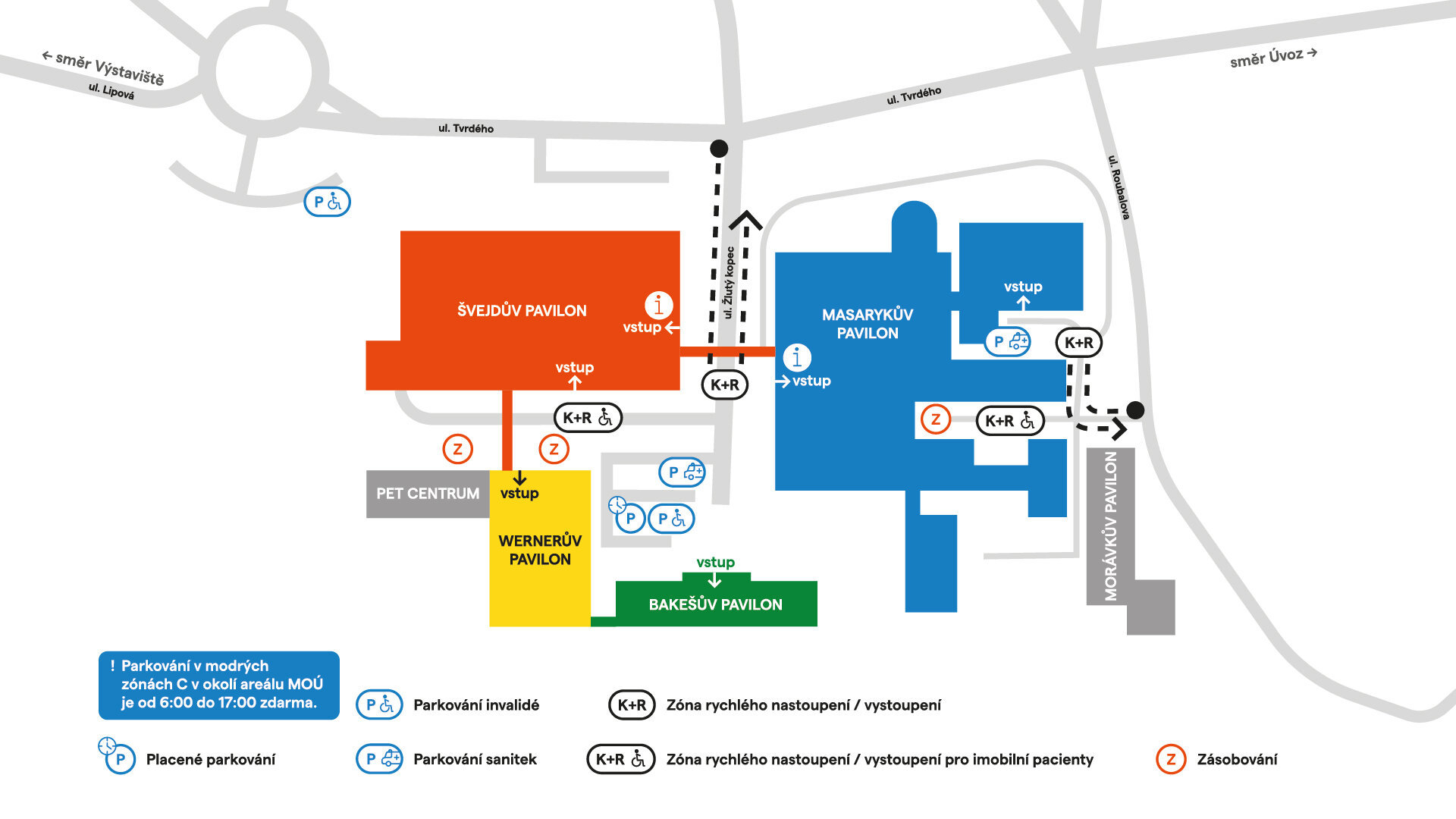
Masarykův onkologický ústav
Žlutý kopec 7
656 53 Brno
Česká republika
T +420 543 131 111
E [obfuscate_1_|99|96|106|97|90|115|55|101|107|108|45|90|114] (Kancelář ředitele)
E [obfuscate_1_|101|88|99|112|108|113|88|91|97|55|108|102|109|42|90|121] ( Ekonomický odbor)
E [obfuscate_1_|110|103|93|105|55|108|102|109|42|90|121] (Oddělení personální a mzdové)
E [obfuscate_1_|100|91|109|95|92|109|107|106|113|100|63|100|103|113|37|98|113] (pro pacienty)
IČO: 00209805
DIČ: CZ00209805
Bankovní spojení: 87535621/0710
SWIFT: CNBACZPP
IBAN: CZ5807100000000087535621
Identifikátor datové schránky: 7vqnyc6
FAX: 543132455 (sekretariát KKOP)